Prevencijas nozīme gastroenteroloģijā: no riska izvērtēšanas līdz agrīnai diagnostikai
Gremošanas sistēmas slimības būtiski ietekmē sabiedrības veselību, tādēļ mūsdienu medicīnā arvien lielāka uzmanība tiek pievērsta preventīvai pieejai, kas vērsta uz slimību riska faktoru agrīnu identificēšanu un savlaicīgu diagnostiku. Gastroenteroloģijā šāda pieeja ir īpaši nozīmīga, jo daudzas patoloģijas ilgstoši var noritēt bez izteiktiem klīniskiem simptomiem, bet savlaicīga to atklāšana ļauj uzlabot ārstēšanas rezultātus un mazināt komplikāciju risku.
Šajā rakstā dr. Linda Anarkulova, GASTRO CENTRA ārste rezidente gastroenteroloģijā, analizē prevencijas nozīmi gastroenteroloģijā, raksturo primārās, sekundārās un terciārās prevencijas principus, kā arī aplūko riska faktoru izvērtēšanas, skrīninga un agrīnas diagnostikas nozīmi klīniskajā praksē.
Mūsdienu veselības aprūpē arvien skaidrāk iezīmējas nepieciešamība pārorientēt fokusu no jau attīstītu slimību ārstēšanas uz savlaicīgu slimību novēršanu un riska faktoru mazināšanu. Profilakse un agrīna diagnostika ļauj būtiski ietekmēt slimības gaitu un ilgtermiņa iznākumus, padarot preventīvo medicīnu par neatņemamu mūsdienu veselības aprūpes sastāvdaļu [1].
Gastroenteroloģijā preventīvai pieejai ir īpaša nozīme, jo daudzas gremošanas sistēmas slimības attīstās pakāpeniski un ilgstoši var noritēt bez klīniski izteiktiem simptomiem. Šādā kontekstā prevencija nozīmē atteikšanos no simptomu gaidīšanas kā galvenā diagnostiskā principa un pāreju uz strukturētu riska faktoru izvērtēšanu un mērķtiecīgu izmeklēšanu kolorektālā vēža un hronisku aknu slimību gadījumā [2,3]. Līdzīga pieeja ir attiecināma arī uz augšējā gremošanas trakta priekšvēža stāvokļu diagnostiku un uzraudzību [9,14].
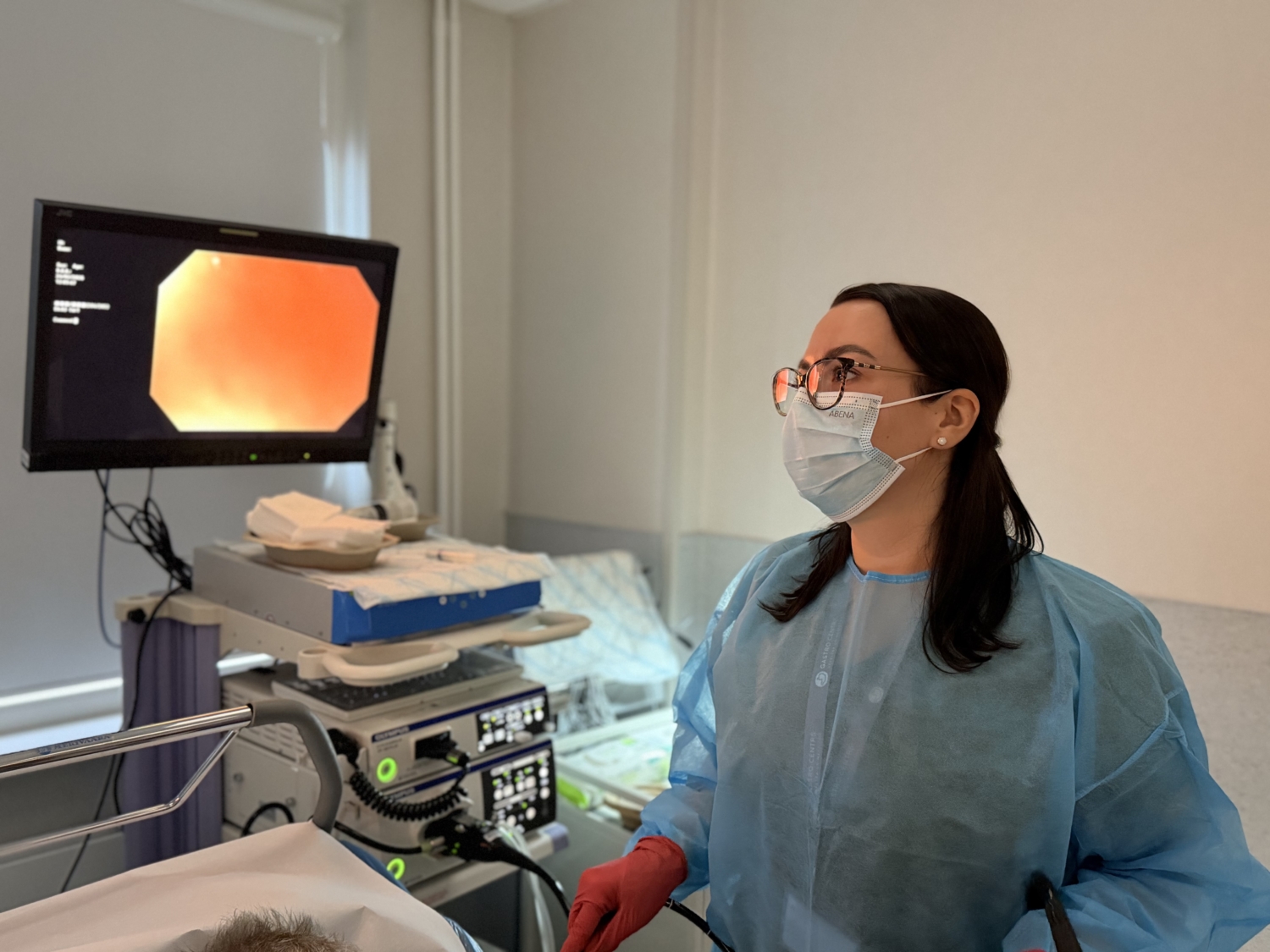
Linda Anarkulova. Foto: Mārtiņš Plūme
Klasiski prevencija tiek iedalīta primārajā, sekundārajā un terciārajā līmenī, un šis iedalījums ir plaši izmantots sabiedrības veselības un klīniskajā praksē. Primārā prevencija ir vērsta uz slimību riska faktoru mazināšanu vēl pirms patoloģiska procesa attīstības, sekundārā prevencija – uz slimību agrīnu atklāšanu un savlaicīgu ārstēšanu, savukārt terciārā prevencija – uz komplikāciju un slimības progresijas ierobežošanu pacientiem ar jau diagnosticētām saslimšanām. Šis klasiskās prevencijas modelis ir piemērojams arī gastroenteroloģijā, kur viena un tā pati izmeklēšanas metode var kalpot gan agrīnai patoloģijas atklāšanai, gan savlaicīgai ārstēšanai un slimības progresijas riska mazināšanai [16].
Kolorektālā vēža skrīnings ir viens no vislabāk pētītajiem sekundārās prevencijas piemēriem klīniskajā praksē. Vadlīnijas uzsver, ka skrīnings jāuzsāk noteiktā vecumā neatkarīgi no simptomu klātbūtnes, jo kolorektālais vēzis agrīnā stadijā bieži norit asimptomātiski [4,6]. Latvijā valsts organizētajā skrīninga programmā kā sākotnējā metode tiek izmantots slēpto asiņu tests fēcēs, kas ļauj identificēt personas ar nepieciešamību turpmākai izmeklēšanai. Vienlaikus būtiski uzsvērt, ka negatīvs testa rezultāts neizslēdz patoloģijas klātbūtni un nav šķērslis kolonoskopijas veikšanai gadījumos, kad pastāv individuāli riska faktori, piemēram, ģimenes anamnēze vai citi klīniski apsvērumi [4,5]. Vairākās valstīs kolorektālā vēža skrīninga pamatmetode jau sākotnēji ir kolonoskopija, kas ļauj ne tikai savlaicīgi diagnosticēt patoloģiskas izmaiņas, bet arī endoskopiski noņemt adenomatozus polipus, tādējādi samazinot kolorektālā vēža attīstības risku [6].
Svarīgi uzsvērt, ka skrīnings un prevencija gastroenteroloģijā nav sinonīmi jēdzieni. Skrīnings ir strukturēts instruments noteiktu slimību agrīnai atklāšanai populācijas līmenī, savukārt prevencija ir plašāks, uz riska faktoru identificēšanu un mazināšanu vērsts process, kas ietver individuālu riska faktoru izvērtēšanu un personalizētu izmeklējumu stratēģiju. Praksē tas nozīmē, ka arī ārpus valsts organizētām skrīninga programmām nozīmīga loma pacientu riska izvērtēšanā un izmeklējumu indikāciju noteikšanā ir gan primārās aprūpes ārstiem, gan gastroenterologiem. Vecums, ģimenes anamnēze, vielmaiņas rādītāji un iepriekšējo izmeklējumu rezultāti bieži sniedz pietiekamu pamatojumu mērķtiecīgai izmeklēšanai pat tad, ja formālie skrīninga kritēriji vēl nav sasniegti, ļaujot pāriet no pasīvas novērošanas uz aktīvu slimības riska mazināšanu un savlaicīgu iejaukšanos [1,4,6].
Individuāla riska izvērtēšana ir būtiska efektīvas prevencijas sastāvdaļa. Ģimenes anamnēze un citi klīniski riska faktori var pamatot agrāku un biežāku izmeklēšanu nekā paredzēts populācijas skrīninga programmās [6,7]. Pastiprināta uzraudzība nepieciešama arī pacientiem ar iekaisīgām zarnu slimībām, jo ilgstošs hronisks iekaisums palielina kolorektālā vēža risku, un regulāra endoskopiska novērošana ir nozīmīga terciārās prevencijas sastāvdaļa [8].
Preventīvās gastroenteroloģijas kontekstā augšējai endoskopijai ir būtiska nozīme augšējā gremošanas trakta gļotādas izmaiņu savlaicīgā atklāšanā un uzraudzībā. Atrofisks gastrīts un intestināla metaplāzija ir klīniski nozīmīgi priekšvēža stāvokļi, kas saistīti ar paaugstinātu kuņģa vēža attīstības risku un bieži norit bez izteiktiem simptomiem [14]. Šo izmaiņu patoģenēzē būtiska nozīme ir Helicobacter pylori infekcijai, kas ir galvenais hroniska gastrīta un ar to saistīto atrofisko izmaiņu riska faktors. Mērķtiecīga eradikācijas terapija samazina kuņģa vēža attīstības risku [15]. Savukārt barības vadā gastroezofageālā atviļņa slimības izraisītas gļotādas izmaiņas, tostarp Barreta barības vads, ir saistītas ar paaugstinātu barības vada adenokarcinomas risku un prasa strukturētu endoskopisku uzraudzību [9].
Prevencija gastroenteroloģijā neaprobežojas tikai ar endoskopiskajiem izmeklējumiem. Būtiska nozīme ir arī laboratoriskajiem izmeklējumiem un attēldiagnostikai, īpaši hronisku aknu slimību kontekstā. Vēdera dobuma ultrasonogrāfija ir plaši pieejama un neinvazīva metode, kas klīniskajā praksē tiek izmantota aknu steatozes un strukturālu aknu izmaiņu izvērtēšanai pacientiem ar metaboliskiem riska faktoriem [12]. Kombinācijā ar laboratoriskajiem rādītājiem tā ļauj identificēt iespējamu hronisku aknu slimību agrīnā stadijā. Riska stratifikācijā papildus nozīme ir neinvazīviem fibrozes novērtēšanas rīkiem, piemēram, FIB-4 indeksam un elastogrāfijai, kas palīdz noteikt pacientus ar progresējošas aknu slimības risku un nepieciešamību turpmākai padziļinātai izvērtēšanai [10,12].
Mūsdienu gastroenteroloģijā aknu steatoze un ar to saistītie aknu bojājumi tiek aplūkoti metaboliskās disfunkcijas asociētas steatotiskas aknu slimības (MASLD) kontekstā. Šis jēdziens atspoguļo ciešo saistību starp aknu bojājumu un metaboliskajiem riska faktoriem, tostarp aptaukošanos, insulīna rezistenci, 2. tipa cukura diabētu un dislipidēmiju. MASLD agrīnā stadijā bieži norit asimptomātiski, tomēr daļai pacientu iespējama progresija līdz fibrozei, cirozei un hepatocelulārai karcinomai. Tas uzsver agrīnas metabolisko riska faktoru atpazīšanas, regulāras laboratorisko rādītāju izvērtēšanas un strukturētas aknu stāvokļa uzraudzības nozīmi [10–12].
Metaboliskie riska faktori ietekmē ne tikai aknu slimību attīstību, bet ir saistīti arī ar paaugstinātu kolorektālā vēža, žultsakmeņu slimības un citu hronisku gastroenteroloģisku patoloģiju risku. Tas uzsver nepieciešamību prevenciju gastroenteroloģijā skatīt plašāk – kā strukturētu pacienta veselības izvērtēšanu, kurā demogrāfiskie, ģenētiskie un metaboliskie faktori, kā arī laboratorisko izmeklējumu un attēldiagnostikas rezultāti tiek analizēti kopumā, nevis izolēti [11,13].
Būtisks prevencijas aspekts ir pacientu izglītošana un skaidra komunikācija par to, ka profilaktiskie izmeklējumi tiek rekomendēti atbilstoši vecumam un individuālajam riskam neatkarīgi no subjektīvu sūdzību klātbūtnes. Tas veicina pacienta informētību un līdzdalību lēmumu pieņemšanā, kā arī atbilst skrīninga vadlīnijās uzsvērtajai nepieciešamībai informēt pacientus par profilaktisko izmeklējumu nozīmi [4,5].
Tādējādi prevencija gastroenteroloģijā nav atsevišķs ārstēšanas posms, bet neatņemama klīniskās prakses sastāvdaļa. Strukturēta, pierādījumos balstīta un individuāli pielāgota pieeja ļauj savlaicīgi identificēt slimību riskus, mazināt komplikāciju attīstību un saglabāt pacientu veselību ilgtermiņā.
Atsauces:
- World Health Organization.Global Action Plan for the Prevention and Control of Noncommunicable Diseases 2013–2030: Progress Update 2023. World Health Organization; 2023.
- Cianci N, Cianci G, East JE. Colorectal cancer: prevention and early diagnosis.Best Pract Res Clin Gastroenterol. 2024;68-69:101876. doi:10.1016/j.bpg.2024.101876
- Asrani SK, Devarbhavi H, Eaton J, Kamath PS. Burden of liver diseases in the world.J Hepatol. 2019;70(1):151-171. doi:10.1016/j.jhep.2018.09.014
- US Preventive Services Task Force. Screening for colorectal cancer: US Preventive Services Task Force recommendation statement.JAMA. 2021;325(19):1965-1977. doi:10.1001/jama.2021.6238
- European Commission Initiative on Colorectal Cancer (ECICC).European Guidelines for Colorectal Cancer Screening and Diagnosis – Update. European Commission; 2022.
- Shaukat A, Kahi CJ, Burke CA, Rabeneck L, Sauer BG, Rex DK. ACG clinical guidelines: colorectal cancer screening 2021.Am J Gastroenterol. 2021;116(3):458-479. doi:10.14309/ajg.0000000000001122
- Butterworth AS, Higgins JPT, Pharoah P. Relative and absolute risk of colorectal cancer for individuals with a family history: a meta-analysis.Eur J Cancer. 2016;56:35-45. doi:10.1016/j.ejca.2015.11.023
- Magro F, et al. ECCO guidelines on inflammatory bowel disease and malignancies surveillance.J Crohns Colitis. 2022;16(suppl 2):ii1-ii42.
- Weusten B, Bisschops R, Coron E, et al. Endoscopic management of Barrett’s esophagus: ESGE guideline.Endoscopy. 2017;49(2):191-198. doi:10.1055/s-0042-122140
- European Association for the Study of the Liver (EASL). EASL clinical practice guidelines on non-invasive tests for evaluation of liver disease severity and prognosis.J Hepatol. 2021;75(3):659-689. doi:10.1016/j.jhep.2021.05.025
- Rinella ME, Lazarus JV, Ratziu V, et al. A multi-society Delphi consensus statement on new nomenclature for metabolic dysfunction–associated steatotic liver disease (MASLD).Gastroenterology. 2023;165(1):120-133. doi:10.1053/j.gastro.2023.03.001
- European Association for the Study of the Liver, European Association for the Study of Diabetes, European Association for the Study of Obesity. Clinical practice guidelines on metabolic dysfunction–associated steatotic liver disease (MASLD).J Hepatol. 2024. doi:10.1016/j.jhep.2024.01.003
- Keum N, Giovannucci E. Global burden of colorectal cancer: emerging trends and risk factors.Nat Rev Gastroenterol Hepatol. 2019;16:713-732. doi:10.1038/s41575-019-0189-8
- Pimentel-Nunes P, et al. MAPS II: ESGE, EHMSG, and ESP guideline on the management of epithelial precancerous conditions and lesions in the stomach.Endoscopy. 2019;51(4):365-388. doi:10.1055/a-0859-1883
- Malfertheiner P, et al. Management of Helicobacter pylori infection: the Maastricht VI/Florence consensus report.Gut. 2022;71(9):1724-1762. doi:10.1136/gutjnl-2022-327745
- Bonita R, Beaglehole R, Kjellström T.Basic Epidemiology. 3rd ed. World Health Organization; 2019.